El virus Zika és un virus emergent, perquè ara mateix cavalca sobre mosquits del gènere Aedes colonitzant noves zones geogràfiques, però porta entre nosaltres obertament més de 60 anys (s’apunta en un darrer estudi que les tres variants que corren ara; dues d’africanes i una d’asiàtica tenen un origen comú allà pel 1920, però no es pot anar més enllà per ara) i probablement centenars o milers d’anys als seus hostes naturals…que encara no tenim del tot identificats.
La primera descripció de Zika vingué d’un macaco Rhesus, un animal sentinella penjat d’un arbre, en una gàbia, dins un programa de la Fundació Rockefeller per a la recerca sobre la febre groga, als boscos Zika, a Uganda. El 18 de abril de 1947, aquest macaco mostrà símptomes febrils i uns dies després va ser portat al laboratori central a Entebbe, capital d’Uganda. Se li extragué sèrum que s’inoculà a ratolins, per via intracraneal. Als 10 dies tots els ratolins estaven malalts. Dels cervells dels ratolins s’aïlla un agent transmissible filtrable, el virus que ara anomenem Zika. Un apunt, recordem que als virus, en el seus inicis se’ls anomenava agents filtrables per distingir-los dels bacteris que sí quedaven retinguts pels filtres; els virus eren com líquid, que s’escolava a través del filtre i podien seguir transmeten la infecció en el filtrat obtingut.
L’any següent, 1948, Zika també fou aïllat al boscos de Zika de mosquits del gènere Aedes, Aedes africanus. Uns anys després, el 1956, es demostra també que el virus Zika es podia transmetre a través de Aedes aegypti, que fou inoculat experimentalment i fou capaç de transmetre el virus a ratolins i a un mico, en condicions de laboratori. Per cert els investigadors van veure una fase d’eclipsi al mosquit; deixaren que els mosquits s’alimentessin (xuclessin) una sang infectada amb una dosi considerable, de 108, és a dir, 100.000.000 virus per ml de virus Zika. A dia 0, dia d’ingesta, cada mosquit individual contenia vora 105,5, vindrien a ser uns 300.000 virus. Però a dia 5 i a dia 10, els virus no pogueren aïllar-se dels mosquits que tornaren a contenir-lo a concentracions inicials, del ordre de 105,0 a partir de dia 15 i 20 mantenint aquest nivell d’infectivitat fins a dia 60, més de 6 setmanes després. El període d’incubació extrínseca del virus al mosquit, per tant estaria entre els 10 i els 15 dies (recomano molt que llegiu l’entrada … https://comentarisviruslents.org/2015/12/27/comentaris-virus-lents-146-competencia-vectorial-o-quan-la-competencia-ens-fibla-de-veritat/).
Tanmateix aquest experiment demostrava la possibilitat de transmissió laboratorial però no ecològica ja que no tenim dades reals i consistents dels nivells de virèmia als animals (primats no humans i humans); si els nivells d’aquesta virèmia fossin baixos potser aquest experimenta erraria ja en el plantejament inicial.
Les inicials proves serològiques fetes a població humana en el veïnatge del aïllament del virus, Àfrica Central, donarem detecció d’anticossos neutralitzants en front de Zika en un 6% (6 de 99 individus) de la mateixa. Una proporció aproximament idèntica a la que es troba en micos, per cert (1 positiu de 15 analitzats).
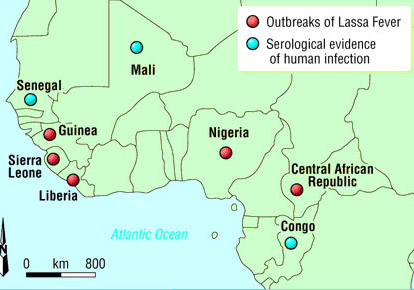
Entre 1951 i 1981, evidència serològica de la infecció per Zika en poblacions humanes ha estat descrita a Uganda, Tanzània, Sierra Lleona, República Centreafricana, Gabon Egipte, i saltant continent a l’Índia, Malàisia, Tailàndia, Filipines i Indonèsia i Vietnam. La prevalença d’anticossos neutralitzants és força variable. Així, a Nigèria, on Zika va ser aïllat de població humana en estudis realitzats en 1968 i entre 1971-1975, el 40% de les persones tenien anticossos neutralitzants en front el virus. Això sí, el 50% en tenia contra la febre groga i de 46% contra West Nile Virus, la qual cosa podria reflectir una circulació més intensa d’aquest dos darrers virus entre la població. Diferencialment, a Lombok, Indonèsia, un estudi serològic posterior va indicar que 9 de 71 (13%) voluntaris humans tenien anticòs neutralitzant enfront ZIKV, la qual cosa podria rflectir una circulació menys intensa…o més recent. En aquest mateix estudi es van analitzar també sèrums de cavalls, bovins, caprins, ànecs, pollastres, aus silvestres, ratpenats i rates en la mateixa localització enfront diversos virus com el virus de la encefalitis japonesa, Chikungunya, Ross River i Zika. Pel que fa a Zika no es detectà positivitat.
A nivell de mosquits, ZIKV ha estat aïllat d’Ae. africanus, Ae. apicoargenteus, Ae. luteocephalus, Ae. aegypti, Ae vitattus i Ae. Hensilii, l’espècie de mosquit predominant present en Yap durant el brot de la malaltia ZIKV el 2007. Tanmateix, pel que fa a aquest darrer, no hi ha lligam epidemiològic provat perquè els investigadors no van poder detectar ZIKV en cap moscards a l’illa durant el brot.

Sembla evident que els primats són (som) susceptibles a l’infecció, i per tant poden mostrar simptomatologia clínica i generen anticossos. A l’inici del seu aïllament es va comprovar que altres especies com rates, conillets d’indies i conills no mostraven signes clínics de la infecció després de la inoculació intracraneal, en condicions de laboratori, de virus Zika. Tanmateix aquesta no és la via normal d’entrada que seria picada de mosquit infectat fora del cervell. I tampoc es va estudiar la presència d’anticossos neutralitzants. Recordem que per a un 80% dels infectats la infecció cursa de forma subclínica, sense simptomatologia aparent. En estudis posterior sí s’han aïllat anticossos de Zika a rosegadors; per tant aquestos animals patirien la infecció i produirien anticossos.
Com veieu, un patchwork d’experiments que quasi plantegen més preguntes que no respostes; ara mateix sabem que Zika es propaga per mosquits i que un vector clar serien els primats no humans…però no podem excloure altres mamífers; estic segur que els mosquits no fan gaires distincions i el virus de ben segur, si en troba un ambient favorable i els receptors cel·lulars adequats, menys. De fet el més probable és que hi hagi un cicle enzootic, un manteniment del virus per part de poblacions de primats no humans i rosegadors i potser altres hostes a les selves originals…que ha derivat en un vessament cap a la població humana. I ara, ben bé es pot dir que Zika ha vingut per quedar-se.
Però aquesta, aquesta és una altra història.

















Comentarios recientes