A diferència del virus de la immunodeficiència humana i els virus de la hepatitis B i C, el perill dels quals, a nivell transfusional, ve de segments de població que funcionen com a transportadors o carriers, amb taxes d’infecció relativament baixes i estables i que poden estar fent donacions sense conèixer el seu status infectiu, molts arbovirus causen curtes virèmies, asimptomàtiques a més, en poblacions amb una incidència infectiva amb grans pics, amb muntanyes i valls, moltes vegades dependents de l’època de l’any, que activa o dorm els seus vectors. Aquesta freqüència variable, estacional dependent de la temperatura i de la pluviositat afegeix una complicació addicional a l’hora de valorar el seu perill transfusional.
No és un tema menor; coneixem molt més d’un centenar d’arbovirus i la majora de ells són susceptibles de transmissió per derivats sanguinis, en tant que generen virèmies significatives. A més, moltes de les infeccions per arbovirus són asimptomàtiques o bé generen un quadre de símptomes difús, amb febre i malestar, poc específic. S’està dient que el 80% aproximadament de les infeccions per Zika son asimptomàtiques; bé, aquest és el mateix percentatge que s’assignava a West Nile Virus l’any 2005 (per més detalls, http://wwwnc.cdc.gov/eid/article/11/8/05-0289b_article). I aquesta gent asimptomàtica no té cap motiu per no continuar fent donacions de sang, entrant sang al circuit. Posem un esquema i treballem sobre aquest…
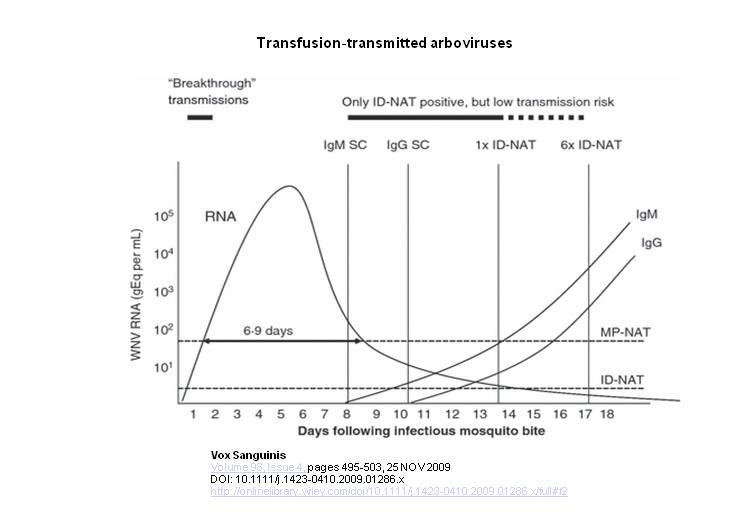
Aquesta gràfica mostra la virèmia i posterior generació d’anticossos en un infectat prototípic de virus de la febre del Nil Occidental (West Nile Virus). Recordem que, ara per ara, la virèmia de Zika està establerta en una setmana aproximadament; la gràfica és del tot escaient. MP-NAT i ID-NAT fan referència a tècniques de detecció d’àcids nucleics del patogen en minipools (MP), o grups de 3-5 donacions; ID-NAT fa referència a les mateixes tècniques aplicades a donació individual; les línies horitzontals en ambdós casos fan referència a la seva capacitat de detecció; allò que estigui per sobre de la línia podrà ser detectat per la tècnica, allò que estigui per sota no, i per tant estarem donant un fals negatiu; un positiu real que donem com a negatiu. La cinètica de distribució normal amb una llarga cua a la dreta fa referència a la virèmia, el nombre de virus per ml, expressat aquí pel seu genoma, ARN. Com veiem puja sense aturador des de la fiblada del mosquit fins a dia 5, s’estabilitza (dia 6) i comença a baixar a plom, de manera que a dia 9 ja es troba per sota del nivell de detecció de les tècniques de MP-NAT. A partir de dia 8 es comença a manifestar o observar la resposta immune humoral mitjançant la producció d’anticossos, inicialment IgM, pocs dies després IgG.
Habitualment, en els centres de donacions i bancs de sang, s’acudeix a tècniques MP-NAT. Si aquesta tècnica s’aplica a un donant asimptomàtic (recordem que el 80% de les infeccions son asimptomàtiques) que està a dia 1, 2 o bé a partir de dia 9 després de la fiblada d’un mosquit carregat de WNV, aquesta sang entrarà en el circuit sense aixecar cap alarma. MP-NAT ens xiula positivitats a partir d’aprox. 102, és a dir, 100 genomes per ml de sang; tot el que estigui per sota no serà detectat. Aquí torna a jugar el seu paper la dosi infecciosa mínima, quina càrrega viral cal per iniciar la infecció. Honestament, no la conec amb certessa, i pot ser molt difícil d’establir perquè probablement és hoste depenent.
Però no divaguem. Tornem a la gràfica; si en lloc de fer servir MP-NAT féssim servir ID-NAT milloraríem força la seguretat (i incrementarien molt el cost dels assajos) però encara i així, durant el primer dia i pels darrers dies de virèmia estaríem donant resultats negatius incorrectes.
Finalment si el nostre infectat desenvolupés simptomatologia, que pel cas de WNV estaria entre 3 i 10-12 dies després de la fiblada del mosquit, encara tindria un període de 3-4 dies, entre la fiblada i l’aparició de febre i altres símptomes, en el que podria donar, i únicament a partir de dia 2, altre cop, les tècniques MP-NAT el detectarien. A partir de la manifestació dels símptomes s’entén, per responsabilitat, que ni el donant doni sang ni el centre de donants li accepti la donació; les tècniques, doncs no s’aplicarien al no haver donació.
Per tant, i com a comentari general, és impossible que en una població amb una certa afectació d’infecció arboviral no entrin algunes donacions que continguin virus infecciosos.
Com podríem preparar-nos abans i durant un gran brot?
Amb un seguit de mesures: assaig de les donacions per NAT (nucleic acid tecniques; en altres paraules detecció per amplificació d’àcids nucleics de seqüències específiques dels virus que estem cercant; preferentment assajos multiplexs que permetin amb una sola reacció detectar o no múltiples patògens alhora); aquestes NAT podrien aplicar-se a minipools en períodes tranquils però quan estiguéssim en un episodi d’increment de circulació arboviral de la població caldria passar a ID-NAT; desenvolupant i mantenint al llarg del temps sistemes de vigilància capaços de detectar infeccions transfusionals; i fent investigacions retrospectives sobre els receptors de productes sanguinis de donants pels que s’acaben confirmant infeccions arbovirals.
Però també, en un brot desfermat, quan i on (mitjançant un algoritme de risc) cal aturar les donacions o recol·lecció de sang i a on recorrerem per mantenir el subministrament; en situacions més calmades, abans d’un brot, com ajornar donacions de persones que han viscut o han viatjat a àrees epidèmiques (per exemple, ara mateix Canadà estableix un període de 21 dies, i EEUU de 28 dies, per poder fer donacions si hom ha estat en zona epidèmica de Zika). I en tot moment, mantenir l’eficàcia i eficiència dels mètodes o etapes d’inactivació que es van començar a instaurar amb l’adveniment de la Síndrome de la Immunodeficiència Adquirida (SIDA); aquestes etapes han fet extremadament segurs derivats sanguinis com els factors de coagulació, les immunoglobulines intravenoses, etc., que s’obtenen a partir del plasma. Però cal tenir mètodes eficients i eficaços per a tots els derivats, inclosos aquells més làbils, o amb menys processat, com poden ser els components cel·lulars del fraccionament; plaquetes o eritròcits.
I el repte definitiu; tot això s’ha de fer econòmic, i fàcil tècnicament, per poder-se implantar sense problemes als països afectats que no estan habitualment en una bona situació econòmica.
Però aquesta, aquesta és una altra història.








 La grip, i entre elles la grip espanyola; aquesta pandèmia que arrencà el 1918 afectà fortament als països del tercer món causant la mort (estimada) de 100 milions de persones. Per comparança, solament 20 milions de persones van morir a la Primera Guerra Mundial. La mortalitat s’acarnissà en els joves; la causa de la mort no era estrictament la infecció si no una reacció excessiva, una sobre-reacció del sistema immune, que acabava amb fallada multiorgànica dels malalts. Aquest virus fou una flamarada de mortalitat; escombrà la Terra i va desaparèixer després de 18 mesos.
La grip, i entre elles la grip espanyola; aquesta pandèmia que arrencà el 1918 afectà fortament als països del tercer món causant la mort (estimada) de 100 milions de persones. Per comparança, solament 20 milions de persones van morir a la Primera Guerra Mundial. La mortalitat s’acarnissà en els joves; la causa de la mort no era estrictament la infecció si no una reacció excessiva, una sobre-reacció del sistema immune, que acabava amb fallada multiorgànica dels malalts. Aquest virus fou una flamarada de mortalitat; escombrà la Terra i va desaparèixer després de 18 mesos.  La febre groga és una malaltia hemorràgica aguda que va causar altes xifres de morts als Estats Units (que va sofrir epidèmies urbanes fins el 1905), però també a Espanya (a Catalunya, milers de barcelonins moriren en la epidèmia de 1821) durant els segles XVIII i XIX. El virus de la febre groga no està eradicat; d’acord amb les estimacions de la OMS, n’hi ha més de 200.000 casos anuals i al voltant de 25.000 morts. L’àrea a l’abast del virus (transmès per mosquits) conté al voltant de 1.000 milions de persones. El virus de la immunodeficiència humana (VIH) causant de la Síndrome d’immunodeficiència Adquirida (SIDA) causa entre 1,6 i 1,9 milions de morts anuals. Si tombem la vista enrere a les tres últimes dècades, aquest virus ha causat ja més de 36 milions de morts. El VIH és un lentivirus que va evolucionar en primats africans fa moltíssims anys, durant milions d’anys, fins que va donar el salt als éssers humans en algun moment de la primera meitat del segle XX. Actualment hi ha al voltant de 35 milions de persones infectades, la majoria d’elles vivint a l’Àfrica subsahariana (més de les 2/3 parts del total). Per desgràcia, només la meitat dels pacients, en les estimacions més afalagadores, poden disposar de teràpia antiretroviral.
La febre groga és una malaltia hemorràgica aguda que va causar altes xifres de morts als Estats Units (que va sofrir epidèmies urbanes fins el 1905), però també a Espanya (a Catalunya, milers de barcelonins moriren en la epidèmia de 1821) durant els segles XVIII i XIX. El virus de la febre groga no està eradicat; d’acord amb les estimacions de la OMS, n’hi ha més de 200.000 casos anuals i al voltant de 25.000 morts. L’àrea a l’abast del virus (transmès per mosquits) conté al voltant de 1.000 milions de persones. El virus de la immunodeficiència humana (VIH) causant de la Síndrome d’immunodeficiència Adquirida (SIDA) causa entre 1,6 i 1,9 milions de morts anuals. Si tombem la vista enrere a les tres últimes dècades, aquest virus ha causat ja més de 36 milions de morts. El VIH és un lentivirus que va evolucionar en primats africans fa moltíssims anys, durant milions d’anys, fins que va donar el salt als éssers humans en algun moment de la primera meitat del segle XX. Actualment hi ha al voltant de 35 milions de persones infectades, la majoria d’elles vivint a l’Àfrica subsahariana (més de les 2/3 parts del total). Per desgràcia, només la meitat dels pacients, en les estimacions més afalagadores, poden disposar de teràpia antiretroviral. 

Comentarios recientes