Com vam comentar a l’entrada anterior el dengue és una malaltia molt estesa amb fortes conseqüències socials i sanitàries per a tots els països tropicals i subtropicals i potser aviat, pels països de zones més temperades.
El dengue és una malaltia amb una simptomatologia inicialment de tipus gripal que afecta a les persones independentment de la seva edat (nadons, nens petits, adults), però rares vegades resulta mortal.
Una persona és infectada per picada d’una femella infectada del gènere Aedes. En un 80% dels casos no hi haurà simptomatologia aparent o bé cursarà com una febre sense complicacions. Entre la picada i l’aparició dels primers símptomes, en el cas que es presentin, transcorren entre 4 i 10 dies. Per tant, tot turista que torni de zona endèmica i que comenci a mostrar símptomes passades dues setmanes de la seva tornada difícilment ho serà per culpa del dengue. S’ha de sospitar que una persona pateix dengue quan una febre elevada (40°C), que apareix sobtadament, s’acompanya de dos dels símptomes següents: mal de cap molt intens, dolor darrere dels globus oculars, dolors musculars i articulars, nàusees, vòmits, engrandiment de ganglis limfàtics o erupcions cutànies lleus, granellada (el salpullido castellà), semblant al del xarampió, que es dona en el 50-80% d’aquells que mostren símptomes oberts. Aquests símptomes duren entre 2 i 7 dies, i és el que s’anomena la fase febril, i la majoria dels infectats es recuperen espontàniament.
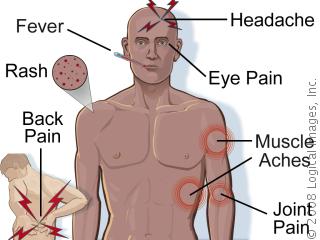
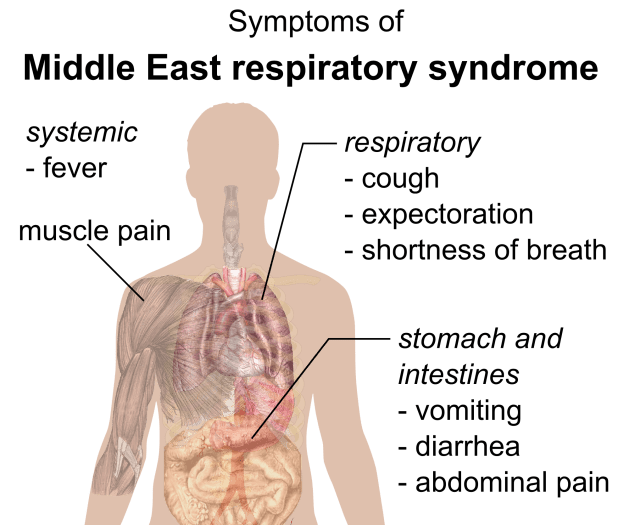
En una petita proporció de casos (el 1% dels infectats) el dengue pot esdevenir dengue greu; és una complicació potencialment mortal perquè cursa amb extravasació de plasma, acumulació de líquids, dificultat respiratòria, hemorràgies greus o falla orgànica. Els signes que adverteixen d’aquesta complicació es presenten entre 3 i 7 dies després dels primers símptomes, és a dir, quan habitualment d’infecció estaria remetent en els casos no greus, i s’acompanyen d’un descens de la temperatura corporal (menys de 38°C) i són els següents: dolor abdominal intens, vòmits persistents, respiració accelerada, hemorràgies de les genives i presència de sang en el vòmit, cansament. Les següents 24 a 48 hores de l’etapa crítica poden ser letals; cal brindar atenció mèdica per evitar altres complicacions i disminuir el risc de mort. Aquesta fase critica és més probable per aquells que s’infecten per segon cop amb un virus dengue de serotip diferent i epidemiològicament semblen més propensos els infants i adolescents. Els que es recuperen d’aquesta fase crítica ho fan reabsorbint els fluids cap el torrent circulatori, en un període de 2-3 dies, amb una millora de rapidesa sorprenent. Ocasionalment aquesta recuperació de fluids pot portar a edemes cerebrals que porten a pèrdues de consciència i convulsions. La fatiga i el cansament es perllongaran per setmanes després de la recuperació.

Crèdits de la imatge: http://nicolemwong.com/design/
Com progressa el virus dengue al nostre cos? El virus entra al cos a través de la pell, dins la saliva del mosquit. Un cop dins s’adhereix i entra dins d’alguns leucocits (glòbuls blancs), concretament les cèl·lules de Langerhans, i es reprodueix dins aquestes cèl·lules dendrítiques mentre aquestes es desplacen dins del cos (recordem que els leucocits són una mena de patrulla de reconeixement i per tant són mòbils). Aquests leucocits infectats, però, produeixen una sèrie de proteïnes d’avís, com interferons i altres citoquines, i aquesta activitat és la responsable dels símptomes no específics com la febre, el mal de cap, el dolor articular i muscular. Els components vírics dins d’aquestes cèl·lules un cop produïts i acoblats en forma de partícula vírica surten per exocitosis (una mena de gemació, arrastrant components cel·lulars). Els virus així alliberats poden entrar en altres leucocits, com monòcits o macròfags. Mentre tant, els interferons i les citoquines activen una resposta innata però també una respost adquirida que suposa la producció d’anticossos contra el virus i l’activació d’uns leucòcits particulars, les cèl·lules T que directament ataquen a les cèl·lules infectades un cop reconegudes. Els anticossos es lligaran fermament a les proteïnes virals de la membrana externa del virus i funcionaran com a llums de guia, senyals moleculars per afavorir la fagocitosi del virus per leucòcits i la seva destrucció. Si la infecció no és aturada, la propagació vírica s’incrementa i arriba a altres òrgans (com el fetge i el moll dels ossos). A aquestes alçades es pot produir una extravasació de líquids del torrent circulatori cap els teixits adjacents, com a conseqüència de malfuncionament de les cèl·lules endotelials (que recobreixen capil·lars i artèries). En conseqüència tindrem menys sang circulant i podem entrar en shock. A més l’afectació del moll de l’ós porta a una trombocitopènia (caiguda en la concentració de plaquetes circulants) que incrementa el risc d’hemorràgies.
No hi ha tractament específic per al dengue. En cas de dengue greu, l’assistència mèdica experimentada pot fer baixar les taxes de mortalitat de més del 20% a menys del 1%. És decisiu mantenir el volum dels líquids corporals per rehidratació oral o intravenosa pels casos lleus i transfusions sanguínies pel casos més greus. De manera oposada, en la fase de recuperació, cal discontinuar l’aport de fluids per evitar un excés d’aquestos que pugi portar a edemes, i si cal, es pot subministrar furosemida https://www.nlm.nih.gov/medlineplus/spanish/druginfo/meds/a682858-es.html).No estan recomanades metodologies mèdiques invasives com intubacions nasogàstriques o injeccions intramusculars o puncions arterials, tenint en compte el perill d’hemorràgies.El tractament de la febre es farà amb paracetamol mentre els antiinflamatoris com l’ibuprofè i l’àcid acetilsalicílic s’evitaran, ja que poden promoure o agreujar el risc d’hemorràgies.
No hi ha cap vacuna llicenciada, al mercat, que protegeixi contra el dengue. S’estan elaborant 3 vacunes vives atenuades tetravalents (com tenim 4 serotips principals de dengue necessitem que la vacuna ens protegeixi dels quatre, d’aquí el “tetra”) que es troben en fase II i fase III dels assajos clínics, i hi ha tres vacunes candidates (basades en plataformes de subunitats, ADN i virus inactivat purificat) en etapes més primerenques de la investigació clínica.
Ara per ara, l’únic mètode per controlar o prevenir la transmissió del virus de la dengue consisteix a lluitar contra els mosquits vectors:

- evitar que els mosquits trobin llocs on dipositar els seus ous, bàsicament aigües estancades i llocs molt humits;
- cobrir, buidar i netejar cada setmana els recipients on s’emmagatzema aigua per a ús domèstic;
- aplicar insecticides adequats als recipients en què s’emmagatzema aigua a la intempèrie;
- utilitzar protecció personal a la llar, com mosquiteres a les finestres, roba de màniga llarga, materials tractats amb insecticides, espirals i vaporitzadors;
- durant els brots epidèmics, les mesures de lluita antivectorial d’emergència poden incloure l’aplicació, per ruixament, d’insecticides;
- vigilància activa dels vectors per determinar l’eficàcia de les mesures de control.
Una malaltia que pot arribar a ser greu i mortal i que tenim ja molt a la vora com a conseqüència del canvi climàtic i de l’expansió dels vectors artròpodes que en són competents. Però, … umm …. què vol dir que un vector sigui competent?
Però aquesta, aquesta és una altra història.



















Comentarios recientes